

深圳市快速抑制COVID-19疫情的非药物干预措施效果评估:基于智能体的建模研究
|
张浩(1989— ),男,河南永城人,博士生,主要从事时空大数据挖掘与基于智能体的传染病建模研究。E-mail: hao.zhang1@siat.ac.cn |
收稿日期: 2021-02-23
要求修回日期: 2021-03-22
网络出版日期: 2022-01-25
基金资助
国家自然科学基金项目(41771441)
国家自然科学基金项目(41901391)
自治区重大科技专项(2020A03004-4)
广东省自然科学基金面上项目(2021A1515011191)
资源与环境信息系统国家重点实验室开放课题(2019)
比尔及梅琳达·盖茨基金(INV-005834)
版权
Effectiveness of Non-pharmaceutical Interventions on Suppressing the 1st Wave of COVID-19 Epidemic in Shenzhen: An Agent-based Modelling Study
Received date: 2021-02-23
Request revised date: 2021-03-22
Online published: 2022-01-25
Supported by
National Natural Science Foundation of China, No(41771441)
National Natural Science Foundation of China, No(41901391)
Major science and technology projects of Xinjiang Uygur Autonomous Region, No(2020A03004-4)
Natural Science Foundation of Guangdong Province, No(2021A1515011191)
State Key Laboratory of Resources and Environmental Information System, No(2019)
Bill & Melinda Gates Foundation, No(INV-005834)
Copyright
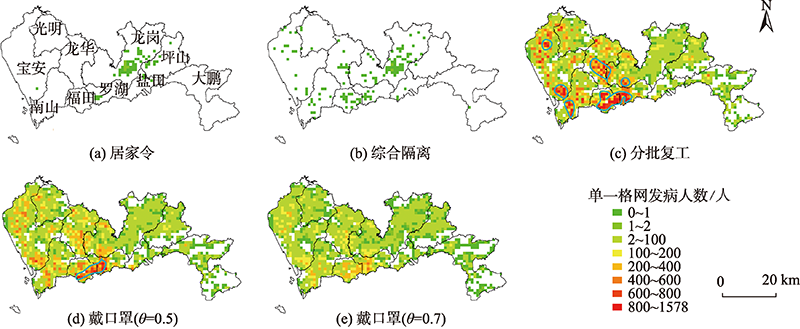
在2020年COVID-19第一波疫情中,通过一系列非药物干预措施,国内许多城市实现了疫情的快速抑制。对这些交叉叠加的多项干预措施进行单项措施的效果评估,识别出关键的防控策略,能够为未来的疫情防控提供重要的经验与科学依据。本研究以深圳市为例,利用融合了多源时空轨迹大数据的空间显式智能体模型评估深圳市快速抑制第一波疫情的各项非药物干预措施效果,识别出核心措施与辅助措施。模拟结果显示,在深圳市第一波疫情中,单项干预措施有效性从高到低依次为居家令、综合隔离、佩戴口罩与分批复工。其中,居家令或综合隔离均能有效抑制疫情的大范围暴发,被本研究称之为核心措施;佩戴口罩或分批复工则只能从不同程度上降低总体感染规模并延缓疫情峰值,并不能抑制疫情暴发,被本研究称之为辅助措施。考虑到社会经济成本以及常态化防疫中人群依从性降低,本研究建议在COVID-19 散发疫情防控中将核心措施与辅助措施相结合,重点实施各项隔离措施,同时将外出佩戴口罩作为疫情常态化防控手段。此外,本研究展示了结合时空大数据与智能体模型精细化模拟城市内部传染病扩散过程的优势:不仅能在城市内部高精度推演疫情发展过程,而且能够支撑评估面向个体及各类型出行活动的非药物干预措施实施效果,为制定针对性、精细化的“时间-空间-人群”防控策略提供重要的科学依据。
张浩 , 尹凌 , 刘康 , 毛亮 , 冯圣中 , 陈洁 , 梅树江 . 深圳市快速抑制COVID-19疫情的非药物干预措施效果评估:基于智能体的建模研究[J]. 地球信息科学学报, 2021 , 23(11) : 1936 -1945 . DOI: 10.12082/dqxxkx.2021.210090
Many cities in China have adopted a series of Non-Pharmaceutical Interventions (NPIs) and rapidly suppressed the 1st wave of COVID-19 epidemic in 2020. It is critical to evaluate the effectiveness of these NPIs for future epidemic control. However, as a variety of NPIs were applied together in practice, it is difficult to evaluate the effectiveness of a single type of intervention by epidemiological observation. Taking Shenzhen city as an example, this study used a spatially explicit agent-based model by integrating mobile phone location data, travel survey data, building survey data and other multi-source spatiotemporal big data to evaluate the effectiveness of different types of NPIs in the suppression of the 1st wave of COVID-19 epidemic in Shenzhen. The simulation results show that the peak of the epidemic would have appeared on the 127th day since Jan 1st of 2020, resulting in an average of 72.26% of the population to be infected without any interventions. In the 1st wave of Shenzhen epidemic, except for the hospitalization of confirmed cases and intercity traffic restrictions, the stay-at-home order was the most effective one, followed by comprehensive isolation and quarantine measures (for close contacts, imported population and suspected cases), mask wearing, and orderly resumption of work. The stay-at-home order and comprehensive isolation and quarantine measures can effectively control the large-scale outbreak of the COVID-19, which are identified as the core measures; Mask wearing and orderly resumption of work can only reduce the overall infection size and delay the epidemic peak, which are identified as secondary measures. Considering the socioeconomic costs and the receding compliance to interventions in the post-epidemic period, this study suggests that the core measures and secondary measures should be combined to control the sporadic cases. Specifically, the local government can give the highest priority to isolation and quarantine measures for confirmed cases and high-risk individuals, complemented by mask wearing. In addition, our model can reveal the high-risk infection areas at a community level, which can help deploy control measures within an urban environment. In summary, this study demonstrated the advantages of integrating spatiotemporal big data and agent-based models to simulate the spread processes of infectious diseases in an urban environment: it can not only simulate the evolving processes of an epidemic at a fine-grained scale, but also evaluate the effectiveness of the NPIs at an individual level and for activity-travel behaviors, which can be useful for precise intervention.

表1 智能体接触类型及接触人数设置Tab. 1 Contact types and daily contact number of individuals |
| 活动类型 | 时空同现人数 | 固定成员人数 | 每天固定接触人数 | 每天随机接触人数 |
|---|---|---|---|---|
| 居家 | 家庭成员数 | 家庭成员数 | 家庭成员数 | - |
| 上学 | 同一幼儿园所有学生 | 同班同学25人 | 同班同学10人 | 其他班级2人 |
| 同一小学所有学生 | 同班同学50人 | 同班同学20人 | 其他班级5人 | |
| 同一初中所有学生 | 同班同学50人 | 同班同学20人 | 其他班级5人 | |
| 同一高中所有学生 | 同班同学50人 | 同班同学20人 | 其他班级5人 | |
| 上班 | 相同工作单位的所有同事 | 工作小组10人 | 工作小组7人 | 其他同事3人 |
| 其他 | 同一建筑从事相同活动的所有个体 | - | - | 受个体接触人数总体分布约束 |
表2 深圳市第一波疫情期间实施的各项非药物干预措施Tab. 2 Non-pharmaceutical Interventions applied by Shenzhen to suppress the 1st wave of COVID-19 |
| 序号 | 措施 | 描述 | 模型实现 | |
|---|---|---|---|---|
| 1 | 集中诊治 | 显性感染者确诊后进行医院集中隔离,直至至恢复;隐性感染者如果核酸检测阳性,则同样集中隔离至核酸检测呈阴性 | 个体从模拟系统中移除 | |
| 2 | 综合隔 离措施 | 密接追踪 | 确诊患者的密切接触者集中隔离14 d* | 对确诊患者的密接者集中隔离14 d,不与任何人产生接触;若密接者未被感染则在14 d后释放,否则从模拟系统移除 |
| 输入人员居家隔离 | 进入城市的人员居家隔离14 d | 仅与家庭成员产生接触 | ||
| 发病后居家隔离 | 具有疑似症状的患者发病后自行居家隔离 | 发病后仅与家庭成员产生接触(病毒传播率下降 ,即模型中的居家隔离有效性) | ||
| 3 | 居家令 | 居民限制外出活动 | 个体仅与家庭成员产生接触 | |
| 4 | 佩戴口罩 | 外出佩戴口罩 | 降低易感者被感染的风险(病毒传播率下降θ,即模型中的口罩有效性) | |
| 5 | 分批复工 | 按时间段和工作性质分批复工 | 有工作的个体从2月10日至3月2日平均分为4批复工,复工前执行居家令 | |
| 6 | 城际交通限制 | 武汉限制外出 | 限制武汉地区人员进入深圳 | 影响模型的潜在输入性病例 |
| 湖北省其他城市限制外出 | 限制湖北省人员进入深圳 | |||
| 限制其余地区入深人员 | 限制其余地区进入深圳的人员数量 | 仅将模型选中的已复工个体放入模拟系统 | ||
注:*确诊患者指核酸检测呈阳性的所有感染者,包含隐性感染者和显性感染者。 |
| [1] |
新华网. 超大型城市战“疫”的深圳样本[ED/OL]. http://www.xinhuanet.com/politics/2020-04/20/c_1125879663.htm,2020-12-01.
[ Xinhuanet. Shenzhen sample of megacity for fight Coronavirus[ED/OL].http://www.xinhuanet.com/politics/2020-04/20/c_1125879663.htm 2020-12-01.]
|
| [2] |
邹旋, 吴永胜, 刘晓剑, 等. 深圳市新型冠状病毒肺炎应急响应策略和措施效果评价[J]. 中华流行病学杂志, 2020, 41(8):1225-1230.
[
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
刘涛, 黎夏, 刘小平. 基于小世界网络的多智能体及传染病时空传播模拟[J]. 科学通报, 2009, 54(24):3834-3843.
[
|
| [13] |
潘理虎, 秦世鹏, 李晓文, 等. COVID-19病毒防控多智能体仿真模型[J]. 系统仿真学报, 2020, 32(11):2244-2257.
[
|
| [14] |
|
| [15] |
|
| [16] |
曹中浩, 张健钦, 杨木, 等. 基于GIS新冠智能体仿真模型及应用——以广州市为例[J]. 地球信息科学学报, 2021, 23(2):297-306.
[
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
深圳市卫生健康委员会. 疫情信息[EB/OL]. http://wjw.sz.gov.cn/yqxx/, 2020-03-31.
[ Shenzhen Municipal Health Commission, Epidemic situation in Shenzhen[EB/OL]. http://wjw.sz.gov.cn/yqxx/, 2020-03-31.]
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
百度. 百度迁徙数据[EB/OL].http://qianxi.baidu.com/, 2020-03-01.
[ Baidu, Baidu mobility data[EB/OL]. http://qianxi.baidu.com/, 2020-03-01.]
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
/
| 〈 |
|
〉 |